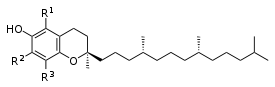
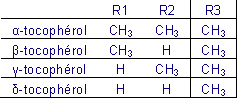
Thermo Scientific étend sa gamme de colonnes pour l’analyse des oligonucléotides. Il s’agit des colonnes DNAPac PA200 RS. Disponibles en 3 dimensions (50 x 4.6 mm, 150 x 4.6 mm et 250 x 4.6 mm), ces colonnes bénéficient d’une technologie à faible diamètre de particules (4 µm) et à forte résistance mécanique (elles peuvent supporter des pressions allant jusqu’à 750 bars/11 000 psi). Ces phases échangeuses d’anions utilisent la même chimie que les DNAPac PA200 existantes dont les particules ont un diamètre de 8 µm.
De manière tout à fait attendue, plusieurs exemples présentés mettent en évidence un gain d’efficacité sur la colonne RS (4 µm) par rapport à l’ancien support (8 µm) en particulier sur les oligonucléotides.
Par contre, le gain de résolution évoqué, n’est pas très évident sur les chromatogrammes présentés, notamment sur la séparation de 7 anions où la concentration injectée semble plus importante sur la colonne 8 µm ce qui, bien sur, peut dégrader la résolution observée.
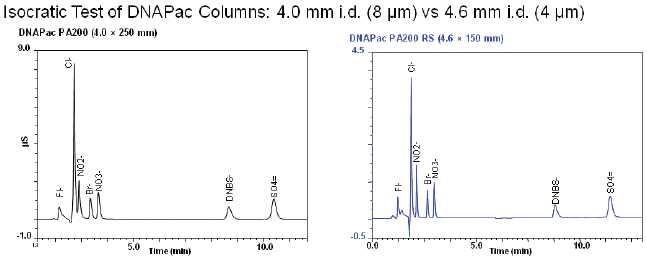
En effet, le transfert à une colonne de plus faible diamètre de particule se traduit généralement par une augmentation de la hauteur de pic et une diminution de la largeur pour une même concentration injectée (à condition que la colonne ai une capacité suffisante).
L’intérêt majeur de ces colonnes échangeuses d’anions réside dans leur résistance à la pression (750 b) ce qui ouvre le champ d’utilisation aux systèmes UHPLC.
Source : J.R. Thayer et al., Performance Improvements for High Resolution Anion-Exchange Oligonucleotide Separations Using Small Particle Substrates, Thermo Scientific Poster Note-PN70515_E01/13S