Commercialisée depuis 2005 par Thermo, la technologie Orbitrap n’était jusqu’à présent disponible qu’en couplage LC (Liquid Chromatography).
Avec la sortie du nouveau Q Exactive Orbitrap GC-MS/MS, Thermo permet aux utilisateurs de chromatographie en phase gazeuse de bénéficier des performances de l’Orbitrap.
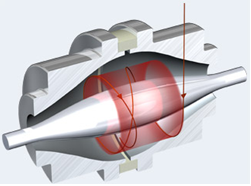
Propriété exclusive de Thermo, l’Orbitrap a été développé par le physicien russe Alexander Makarov en 1999. Le principe du piège orbitalaire est semblable à celui des autres trappes d’ions. Lorsqu’ils sont dans la trappe, tous les ions engagent une trajectoire identique autour de l’«olive ». En revanche, leur vitesse varie en fonction de leur masse.
Ce spectromètre affiche des performances de résolution pouvant aller de 60 000 à 120 000 (pour un rapport m/z de 200). Pour rappel cette résolution est le rapport m/Dm où Dm représente l’écart de masse entre le pic d’interêt et son voisin le plus proche. Cette résolution permettra d’accéder à la masse exacte des molécules. Il est toutefois important de noter que la précision en masse ne fournira la masse exacte qu’à la condition que le spectromètre ait été étalonné avec précision (!).
Généralement, ces spectromètres dits, à haute résolution, sont davantage utilisés pour des études d’élucidation structurales. La quantification de molécules dans des échantillons semble néanmoins possible. En effet, les performances annoncées pour cet appareil en mode full scan sont comparables à celles d’un triple quadripôle opérant en mode SRM (Selected Reaction Monitoring). La limite de détection est de l’ordre du ppt.
Si les performances de l’Orbitrap ne sont plus à démontrer, le coût élevé de ces appareils ne permettra hélas pas à tous les laboratoires de s’équiper…





 Les auteurs nous rappellent que l’utilisation du CO2 comme phase mobile peut présenter des difficultés d’élution pour les composés polaires et de haut poids moléculaire. Afin d’augmenter le pouvoir solvant de la phase mobile et de favoriser la solubilité de ces composés, plusieurs co-solvants peuvent être utilisés. Le méthanol est le co-solvant le plus courant pour l’élution des composés polaires. Plus généralement les alcools (caractère donneur d’hydrogène) sont des co-solvants de première intention car ils permettent une grande efficacité sans trop dégrader la sélectivité.
Les auteurs nous rappellent que l’utilisation du CO2 comme phase mobile peut présenter des difficultés d’élution pour les composés polaires et de haut poids moléculaire. Afin d’augmenter le pouvoir solvant de la phase mobile et de favoriser la solubilité de ces composés, plusieurs co-solvants peuvent être utilisés. Le méthanol est le co-solvant le plus courant pour l’élution des composés polaires. Plus généralement les alcools (caractère donneur d’hydrogène) sont des co-solvants de première intention car ils permettent une grande efficacité sans trop dégrader la sélectivité.