En SFC, l’état physique du CO2 supercritique, et en particulier sa masse volumique, a une influence sur sa polarité et donc sur la rétention des composés [1].
Pour moduler cette polarité, il convient de faire varier la pression et/ou la température du fluide. Lorsque la masse volumique décroit (donc que la pression diminue), le facteur de capacité (caractérisant la rétention) augmente. Ce phénomène est indépendant de la nature du soluté et de la phase stationnaire, il peut s’expliquer essentiellement par la variation des interactions soluté-phase mobile [2].
Lors d’un précédent post (16 mai 2013), nous avons présenté des résultats obtenus sur la séparation de 2 composés génotoxiques : le 1,2-dibromoéthane et 1-bromo-2-chloroéthane dans des conditions fixes de température (65°C) et de pression (2000 psi).
Pour évaluer l’effet de la pression et de la température sur la séparation de ces composés, nous avons fait varier la pression de sortie du CO2 (de 1500 psi à 3500 psi) en condition isotherme (65°C), puis la température de colonne (de 15°C à 75°C) en condition isobare (2000 psi). L’étude se déroule sur un appareil UPC²™ de Waters®.
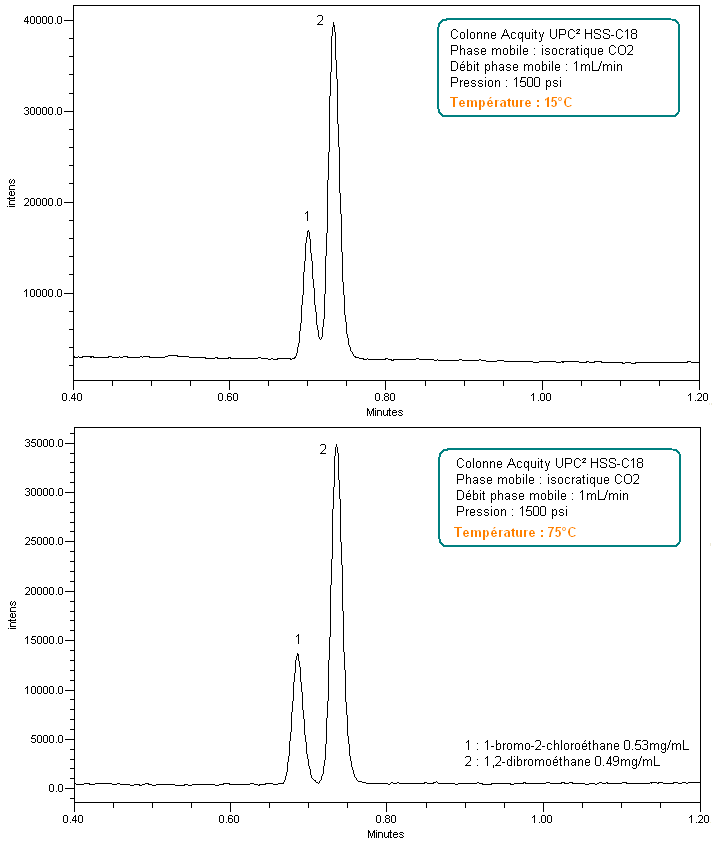
Sur les chromatogrammes, on peut constater que la température ne modifie que très faiblement les temps de rétention du 1-bromo-2-chloroéthane (0,701 min à 15°C et 0,686 min à 75°C) tandis que celui du 1,2-dibromoéthane reste constant (0,733 min à 15°C et 0,736 min à 75°C).
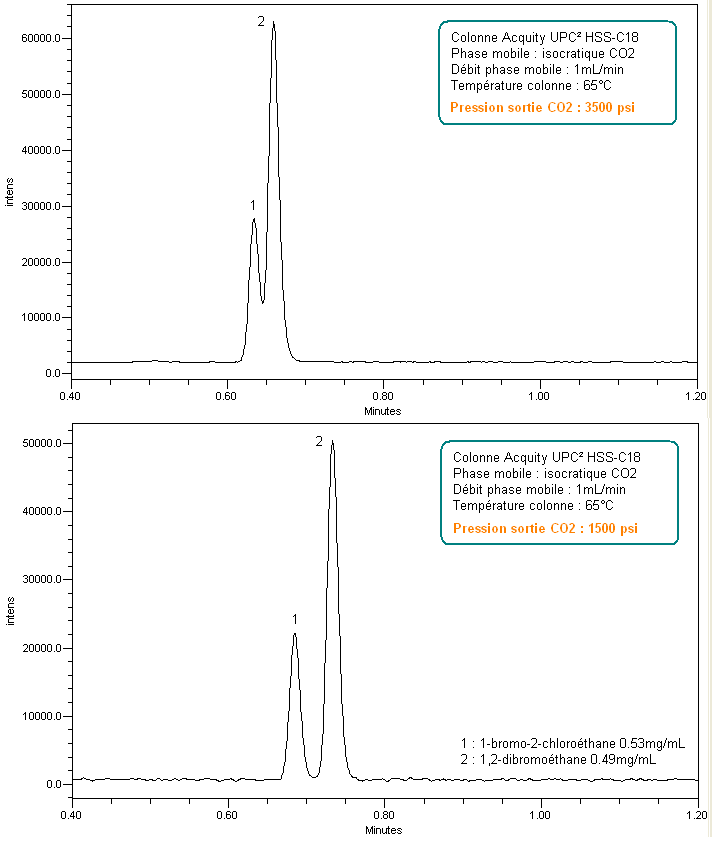
A l’inverse, l’effet de la pression est très net sur les temps de rétention (décalage de temps de rétention de l’ordre de 0,5 min).
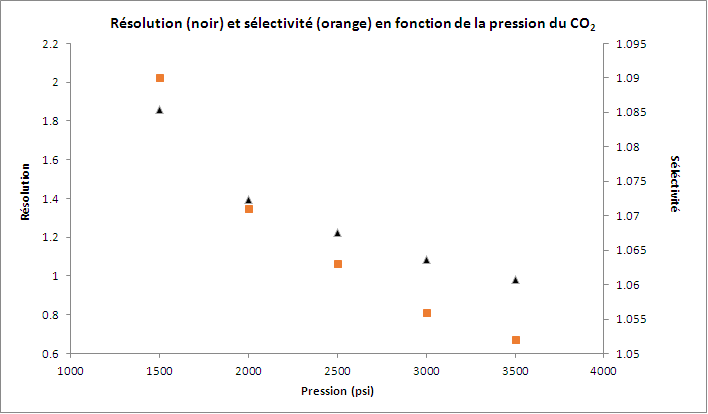
La résolution et la sélectivité entre les deux composés en fonction de la pression sont des fonctions décroissantes. L’écart maximal atteint 89 % sur la résolution et 4 % sur la sélectivité.
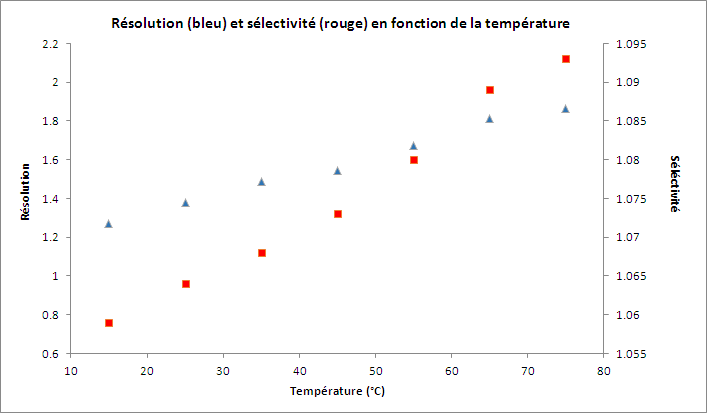
Ce sont en revanche des fonctions croissantes en fonction de la température. l’augmentation est de 47 % sur la résolution et de 3 % sur la sélectivité.
La meilleure résolution est obtenue à faible pression (1500 psi) et haute température (75°C).
L’ analyse de l’efficacité montre une influence semblable de la pression et de la température (environ 13%). Par contre le facteur de capacité croit de 14 % avec la diminution de la pression alors qu’il n’évolue que de 4 % sous l’influence de la température. Cette observation est en accord avec l’hypothèse d’une modification de la polarité du CO2 lors du changement de pression entraînant une variation des interactions soluté-phase mobile [2].
[1] R. Rosset, M. Caude et A. Jardy, Chromatographies en phase liquide et supercritique (Masson – 1991)
[2] P. Mourier, M. Caude, R. Rosset, Analusis, 13, 299, 1985
